باتری سدیم یونی(قسمت دوم)
مقدمه
در قسمت قبل به نکات کلی باتری سدیم یون پرداختیم و در این قسمت قصد داریم به صورت جزئی تر با باتریهای بر پایهی سدیم بیشتر آشنا بشویم و نحوهی عملکرد آن را بررسی نماییم.
اجزای باتری سدیم یون
همانطور که در شکل 1 دیده می شود، یک باتری سدیم-یونی از پنج قسمت مجزا تشکیل شده است که عبارتند از :
آند
کاتد
الکترولیت
جمعکننده جریان
جداکننده
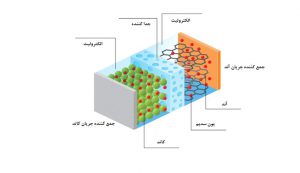
وظیفهی هر یک از این اجزا
کاتد (پایانه مثبت): مهمترین بخش هر باتری سدیم-یونی کاتد آن است. کاتد معمولاً یک ماده سرامیکی یا پلیمری است که دارای پتانسیل الکتریکی بالاتر از آند میباشد. کاتد مهمترین بخش تعیینکننده ظرفیت شارژ باتری است.
آند (پایانه منفی): وظیفهی این بخش نگهداری یونهای سدیم در ساختار خود در حالت شارژ است. آند، مهمترین بخش تعیینکننده میزان پایداری و عمر یک باتری سدیم یونی است.
الکترولیت: الکترولیت یک ماده متراکم (مایع یا جامد) است که بین کاتد و آند قرار میگیرد. وظیفهی آن عبور دهی یونهای سدیم از کاتد به آند و برعکس است.
جداکننده: جداکننده یک غشای متخلخل است که در الکترولیت و بین آند و کاتد قرار میگیرد. وظیفهی اصلی این قسمت، جداسازی کاتد و آند از یکدیگر و جلوگیری از ایجاد اتصال کوتاه است. لذا معمولاً از یک ماده پلیمری و یا سرامیکی عایق الکترون که درعینحال به دلیل متخلخل بودن هادی یون سدیم است بهعنوان جداکننده استفاده میشود.
کلکتور یا جمع کننده جریان: جمع کنندههای جریان برای هدایت الکترونهای ناشی از واکنش شیمیایی داخل باتری به مدار بیرونی استفاده میشوند. کلکتور استفادهشده در کاتد باتریهای سدیمی معمولاً آلومینیم و جمع کننده جریان آند معمولاً آلومینیم یا مس است.
مکانیزم عملکرد باتری سدیم یون: مکانیزم عملکرد باتریهای سدیم یونی همانند نسل قبلی خود یعنی باتریهای لیتیوم یونی است و بهطور شماتیک در شکل 2 نشان داده شده است. در حین دشارژ یا تخلیه این نوع از باتریها، یونهای سدیم از آند جدا میشوند و با عبور از الکترولیت وارد کاتد میگردند. همزمان جریان الکترونها از آند به کاتد نیز برقرار میشود که این جریان انرژی موردنیاز وسایل الکترونیکی را تأمین میکند. در حین شارژ باتری نیز یونهای سدیم از کاتد خارج میشوند و دوباره از طریق الکترولیت بهسوی آند برمیگردند.
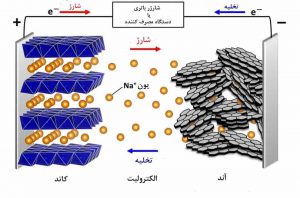
شکل2- شماتیک سیکل های شارژ و تخلیه یک باتری سدیم یونی
مواد الکترودی باتری سدیم یون
الکترودها (کاتد و آند) مهمترین بخشهای یک باتری سدیم یونی هستند و مشارکت این دو با الکترولیت تعیینکننده بسیاری از ویژگیهای باتری همچون ولتاژ، ظرفیت، سرعت شارژ، عمر و… است. بر اساس مکانیزم جذب سدیم، کاتد باتریهای سدیم یونی به دو دسته درجی(intercalation) و تبدیلی(conversion) و آند به سه دسته درجی، تبدیلی و آلیاژی(Alloy) تقسیم میشوند. در مواد الکترودی درجی، یون سدیم در فضای بین لایهای میزبان قرار میگیرد.
در مواد تبدیلی ورود یا خروج یون سدیم منجر به تشکیل ترکیبات جدید میگردد و در مواد آلیاژی وارد شدن سدیم درون شبکه یک ماده، سبب آلیاژی شدن آن ماده میگردد. اکثر مواد الکترودی بهجز تعدادی محدود (نظیر ترکیبات کربنی) به دلیل رسانایی الکتریکی پایین بایستی با مواد رسانای دیگری پوشش داده شده یا کامپوزیتی گردند.
در ادامه بایستی با یک فرآیند چاپ مخصوص، ماده الکترودی روی جمع کنندههای جریان لایه نشانی شود. در ادامه این مبحث به معرفی مواد الکترودی رایج در باتریهای سدیم یونی پرداخته میشود.
کاتد باتری سدیم یون
بهطورکلی باتریهای سدیمی ازنظر ویژگیهای عملکردی و ساختاری شباهت زیادی به باتریهای لیتیوم یونی دارند. همانطور که در بخشهای قبل نیز توضیح داده شد، کاتد مهمترین بخش یک باتری سدیم یونی است. در سالهای اخیر مواد کاتدی مختلفی ازجمله اکسیدهای فلزات واسطه با ساختارهای لایهای و تونلی و همچنین پلیمرها معرفی گردیدهاند.
شکل 3، تعدادی از کاتدهای رایج در این نوع باتریها را در مقایسه با کاتدهای لیتیومی معروف نشان میدهد. همانطور که دیده میشود، کاتدهای لیتیومی بهطورکلی ظرفیت شارژ و ولتاژ بیشتری نسبت به کاتدهای سدیمی نشان میدهند. لذا این موضوع ضرورت سنتز و استفاده از مواد و ساختارهای مدرن در این دسته از باتریها را بیشازپیش نمایان میسازد.
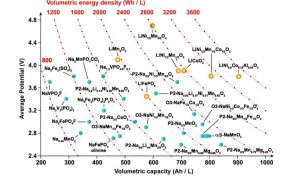
شکل3: ولتاژ بر حسب ظرفیت حجمی در مواد کاتدی رایج در باتری های سدیمی و کاتدهای لیتیومی معروف
آند باتری سدیم یون
آند وظیفهی ذخیرهسازی یونهای سدیم در هنگام شارژ و تحویل آنها به کاتد در هنگام دشارژ را بر عهده دارد. آندها به دو دستهی فلزی و سرامیکی تقسیم میشوند.
یافتن آندی با ولتاژ ذخیره سدیم مناسب، ظرفیت برگشتپذیر بالا و پایداری ساختاری بالا به عنوان مانعی برای توسعه باتریهای سدیم یونی مطرح بوده است.
آندهای فلزی باوجود چگالی انرژی بالا و هدایت الکتریکی زیاد، به دلیل انجام واکنشهای نامطلوب در فصل مشترک آند-الکترولیت بازده باتری را کاهش میدهند. برای مثال واکنشپذیری بالای فلز سدیم خالص با محلول آلی الکترولیتی و تشکیل یک ساختار شاخهای روی آند میتواند از فلز لیتیوم خالص نیز مسئلهسازتر باشد.
همچنین دمای پایین ذوب سدیم (97.7 ͦ C) نیز میتواند مشکلات ایمنی در دماهای محیطی ایجاد نماید. آندهای سرامیکی نیز معمولاً در اثر ورود و خروج یونهای سدیم دچار تغییرات حجمی شدید میگردند که میتواند به تخریب و یا فروپاشی آنها در بلندمدت انجامد. همچنین اخیراً مشخصشده است قابلیت درج سدیم در آند گرافیت کمتر از لیتیوم است. لذا به تحقیقات بسیار بیشتری در حوزه آند احتیاج است.
شکل 4، ظرفیت ویژه بر حسب پتانسیل خروج سدیم برای آندهای مختلف را نشان میدهد. همانطور که دیده میشود در بین تمامی آندهای موجود، فلز سدیم خالص دارای بالاترین ظرفیت است. بهطورکلی آندهای فلزی علاوه بر ظرفیت بیشتر، یون سدیم را نیز راحتتر از دست میدهند که نشاندهنده خواص بهتر آندهای فلزی است درحالیکه بایستی تدابیری برای کاهش اثرات لایه فصل مشترک اندیشیده شود.
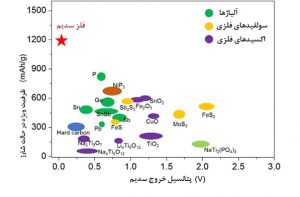
شکل4- مقایسه انواع مختلف آند در باتری های سدیم یونی بر حسب ظرفیت ویژه و پتانسیل خروج سدیم
الکترولیت باتری سدیم یون
استفاده از الکترولیتهای مایع آلی در باتریهای سدیمی با مشکلات ایمنی همراه است و لذا به نوع جدیدی از الکترولیت احتیاج است. رایجترین فرمولاسیون الکترولیت در باتریهای سدیم یونی محلول سدیم کلرات و یا سدیم فسفروفلورید در حلالهای استر کربناتی است.
بااینحال خوردگی فلز سدیم در محلولهای یادشده و ایجاد یک لایه در فصل مشترک آند-الکترولیت میتواند باعث کاهش راندمان باتری گردد. لذا به نظر میرسد، توسعه محلولهای الکترولیتی آبی بهجای محلولهای الکترولیتی آلی ضروری است. علاوه بر این دستهای دیگر از الکترولیتها یعنی الکترولیتهای حالتجامد به دلیل حضور مواد غیر آلی میتوانند بر مشکلات ایمنی غلبه کنند. بااینحال به دلیل هدایت یونی کم و حساسیت بالا به رطوبت کاربرد آنها محدود میگردد.
از سوی دیگر الکترولیتهای پلیمری به دلیل هدایت یونی مناسبتر، نسبت به الکترولیتهای حالتجامد مزیت بیشتری دارند. همچنین به دلیل ژل شدن الکترولیت مایع در زمینه پلیمری، از تراوش جلوگیری میشود و خطر آتشسوزی کاهش مییابد.
جداکننده باتری سدیم یون
جداکننده نقش مهمی در جداسازی کاتد و آند از یکدیگر و عبور دهی یونهای سدیم در محلول الکترولیت دارد. این مسئله شدیداً روی عملکرد باتری همچون ایمنی حرارتی، ایمنی مکانیکی، سرعت عملکرد و عمر اثر میگذارد. لذا لازم است جداکننده خواصی همچون هدایت یونی بالا، مقدار و اندازه تخلخل بهینه، تر شوندگی مناسب با الکترولیت و پایداری حرارتی بالا داشته باشد.
تاکنون چندین ماده مختلف پلیمری، شیشهای و کامپوزیتی بهعنوان جداکننده در باتریهای سدیمی موردبررسی قرار گرفتهاند. از این مواد میتوان به پلیمرهای نفیون و پلیاتیلن، الیاف شیشه و کامپوزیتهای زیرکونیا-پلی اولی فین و سیلس-پلی اولی فین اشاره نمود. تاکنون تحقیقات در مورد جداکننده نسبت به الکترودها و الکترولیت کمتر بوده است و جداکنندههای فعلی راهی طولانی برای رسیدن به الزامات مهندسی در باتریهای سدیم یونی دارند.
جمعکننده باتری سدیم یون
از جمع کنندههای جریان برای انتقال جریان الکتریکی از درون باتری به مدار بیرونی استفاده میشود. جمع کننده جریان بهعنوان جرم و حجم غیرفعال در باتری در نظر گرفته میشود و استفاده از آن چگالی انرژی را کاهش میدهد. از سوی دیگر جمع کننده جریان بایستی در تماس با اجزای باتری پایدار بماند و دچار خوردگی نگردد.
در باتریهای لیتیوم یونی به دلیل واکنش با لیتیوم امکان استفاده از آلومینیم بهعنوان جمع کننده جریان در آند وجود ندارد. اما خوشبختانه این مشکل در باتریهای سدیم یونی وجود ندارد. در باتریهای سدیم یونی به اثر جنس جمع کننده جریان بر عملکرد باتری به مقدار کمی توجه شده است و توجه تنها به دو ماده مس و آلومینیم بوده است.
نتیجه گیری
در این قسمت به صورت کلی عملکرد باتری سدیم یون بررسی شد و دیدیم که اساس کار باتریهای سدیم یون، همانند باتریهای لیتیوم یون است.
مراجع
Wang, S. Song, C. Xu, N. Hu, J. Molenda, L. Lu, Development of solid-state electrolytes for sodium-ion battery–A short review, Nano Mater. Sci. 1 (2019) 91–100. https://doi.org/10.1016/j.nanoms.2019.02.007.
W. Chen, L. Zhang, C. Liu, X. Feng, J. Zhang, L. Guan, L. Mi, S. Cui, Electrospun Flexible Cellulose Acetate-Based Separators for Sodium-Ion Batteries with Ultralong Cycle Stability and Excellent Wettability: The Role of Interface Chemical Groups, ACS Appl. Mater. Interfaces. 10 (2018) 23883–23890. https://doi.org/10.1021/acsami.8b06706.
K. Kubota, S. Komaba, Review—Practical Issues and Future Perspective for Na-Ion Batteries, J. Electrochem. Soc. 162 (2015) A2538–A2550. https://doi.org/10.1149/2.0151514jes.
L. Li, Y. Zheng, S. Zhang, J. Yang, Z. Shao, Z. Guo, Recent progress on sodium ion batteries: potential high-performance anodes, Energy Environ. Sci. 11 (2018) 2310–2340. https://doi.org/10.1039/C8EE01023D.
S. Mukherjee, S. Bin Mujib, D. Soares, G. Singh, Electrode Materials for High-Performance Sodium-Ion Batteries, Materials (Basel). 12 (2019) 1952. https://doi.org/10.3390/ma12121952.
C. Vaalma, D. Buchholz, M. Weil, S. Passerini, A cost and resource analysis of sodium-ion batteries, Nat. Rev. Mater. 3 (2018) 18013. https://doi.org/10.1038/natrevmats.2018.13.
نویسنده: محسن کریم پور
تاریخ انتشار: بهمن 98




با عرض سلام و ادب
میشه لطفا در مورد فرایند sodiation-desodiation در باتری های سدیمی توضیح بفرمایید که ایا با فرایند insertion فرق دارد؟
سلام خدمت شما.
فرایند sodiation-desodiation در باتری های سدیم یون به صوت ساده یعنی این که آند و یا کاتد باتری دارای سدیم شود (sodiation) و یا سدیم از آن خارج شود (desodiation). این فرایند به روش های مختلف اتفاق می افتد که یکی از این روش ها با نام روش insertion معروف است. در این روش سدیم در بین لایه های کاتد و یا آند قرار می گیرد و به صورت ساده می توان گفت که درروش insertion، واکنشی بین سدیم و الکترود آند یا کاتد رخ نمی دهد. دو روش دیگر نیز وجود دارد به نام آلیاژی و تبادلی که به ترتیب با نام های انگلیسی alloying و conversion شناخته می شوند. در ضمن به روش insertion، روش intercalation نیز گفته می شود. برای فهم بهتر این سه روش به آدرس https://rahabattery.ir/انواع-آند-در-باتری%E2%80%8Cهای-لیتیوم-یون/ مراجعه کنید.